Biosimilars
Biosimilars – für einen breiteren Zugangzu hochwirksamen biologischen Therapien
Biosimilars sorgen dafür, dass biologische Arzneimittel erschwinglicher werden. Das verbessert für Patientinnen und Patienten den Zugang zu dringend benötigten Therapien und entlastet gleichzeitig die Budgets der Gesundheitssysteme.
Was sind Biosimilars?
Seit ihrer Einführung in den 1980er-Jahren haben biologische Arzneimittel die Behandlung vieler schwerer Krankheiten revolutioniert. Dazu gehören chronisch-entzündliche Erkrankungen wie Psoriasis oder COPD, Erkrankungen der Netzhaut oder Krebs. Biosimilars sind Nachfolgeprodukte innovativer biologischer Arzneimittel, die nach Ablauf der gesetzlichen Schutzfristen auf den Markt gebracht werden können.
“Ein Biosimilar ist ein biologisches Arzneimittel, das in Bezug auf Struktur, biologische Aktivität sowie Wirksamkeit, Sicherheit und Immunogenitätsprofil (die inhärente Fähigkeit von Proteinen und anderen biologischen Arzneimitteln, eine Immunantwort auszulösen) einem anderen, bereits in der EU zugelassenen biologischen Arzneimittel (dem sogenannten „Referenzarzneimittel“) in hohem Maße ähnlich ist.” — Europäische Arzneimittelagentur1
Biosimilars werden mithilfe modernster Biotechnologie in lebenden Zellen hergestellt. Aufgrund dieses Herstellungsprozesses kann es keine absolut identischen Nachfolgeprodukte eines Referenzarzneimittels geben. Biosimilars sind dem Referenzarzneimittel – das selbst auch von Charge zu Charge geringe Unterschiede aufweist – jedoch sehr ähnlich (similar) und besitzen eine vergleichbare Qualität, Sicherheit und Wirksamkeit. Dies ist die Grundlage für die Zulassung eines Biosimilars in hochregulierten Märkten wie der EU, den USA, Kanada, Japan und Australien.
Vergleich Biosimilar (links) und Generikum (rechts):

BiosimilarsGroße komplexe Moleküle, die aus lebenden Zellen produziert werden
GenerikaMeist kleine synthetische Moleküle
Biosimilar-Entwicklung
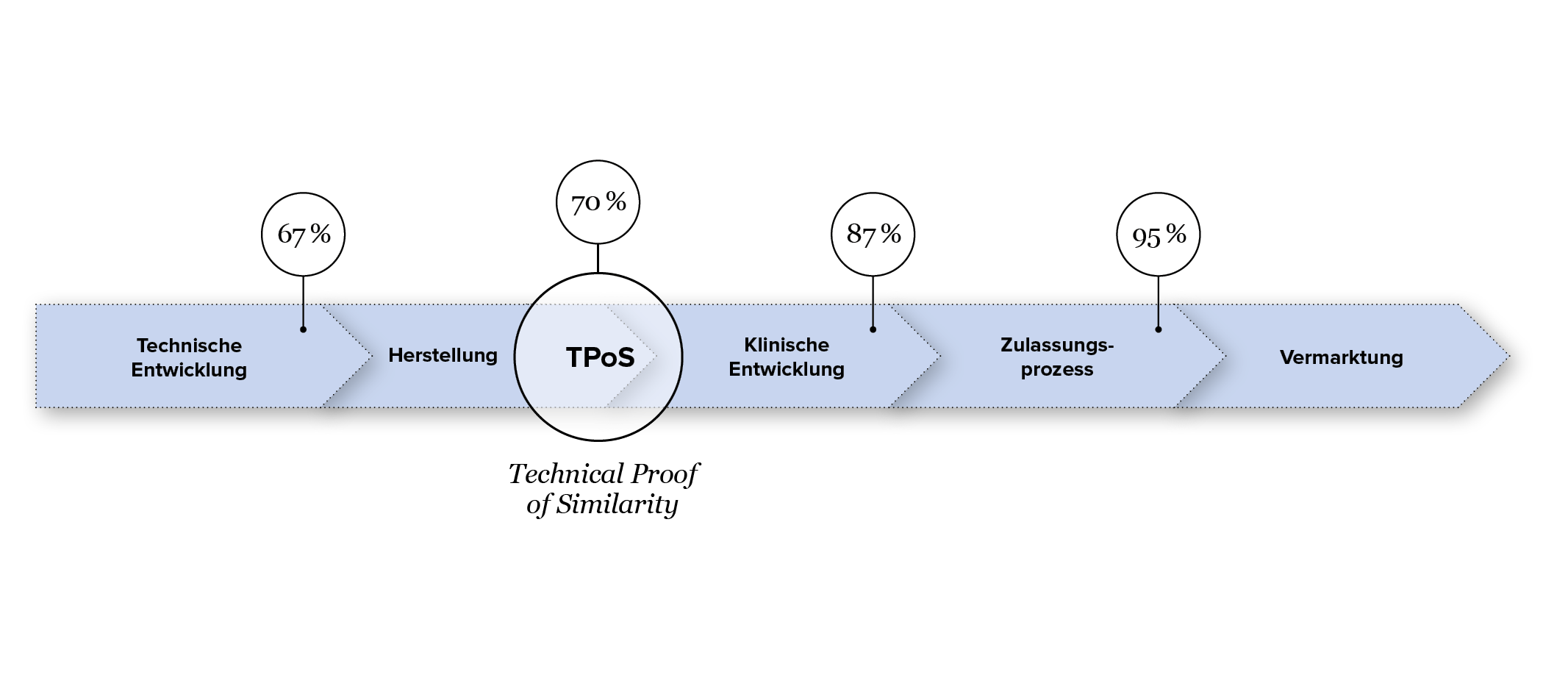
Die hohe Komplexität biologischer Wirkstoffe und ihre spezifischen Herstellungsprozesse erfordern ein besonderes wissenschaftliches und regulatorisches Know-How. Expertinnen und Experten aus rund 30 Nationen und unterschiedlichen Disziplinen arbeiten bei Formycon in der Biosimilar-Entwicklung. Etwa sechs bis acht Jahre liegen zwischen der Auswahl des Moleküls und der Einreichung der Zulassungsunterlagen bei den Arzneimittelbehörden. In diesem Zeitraum folgt die technologisch und wissenschaftlich anspruchsvolle Entwicklung dem Hauptfokus, die vergleichbare Wirksamkeit, Sicherheit und Qualität des Biosimilars zum jeweiligen Referenzprodukt zu belegen.
Dadurch fällt das Entwicklungsrisiko gegenüber der Entwicklung eines innovativen biologischen Wirkstoffs deutlich geringer aus. Schon zum Ende der technischen Entwicklungsphase und mit Erreichen des TPoS (Technical Proof of Similarity) liegt die Erfolgswahrscheinlichkeit – also die Wahrscheinlichkeit, dass der Biosimilar-Kandidat die Zulassung durch die Arzneimittelbehörden erhält – bei 70 %.2
Der Markt für Biosimilars
Biosimilars sind in den 20 Jahren seit ihrer Einführung mehr und mehr zu einer wichtigen Säule der weltweiten Gesundheitssysteme geworden. Denn innovative biologische Arzneimittel sind bei der Behandlung schwerer Erkrankungen zwar sehr effektiv, andererseits aber auch sehr kostspielig. Kommen nach Ablauf der Exklusivität eines innovativen biologischen Arzneimittels Biosimilars auf den Markt sinken die Behandlungskosten in der Regel deutlich.
Allein in Deutschland konnten so für das Jahr 2024 knapp 2 Mrd. Euro eingespart werden – Tendenz steigend.3 Im europäischen Maßstab summieren sich die Einsparungen seit Einführung des ersten Biosimilars im Jahr 2006 auf mehr als 56 Mrd. Euro.4
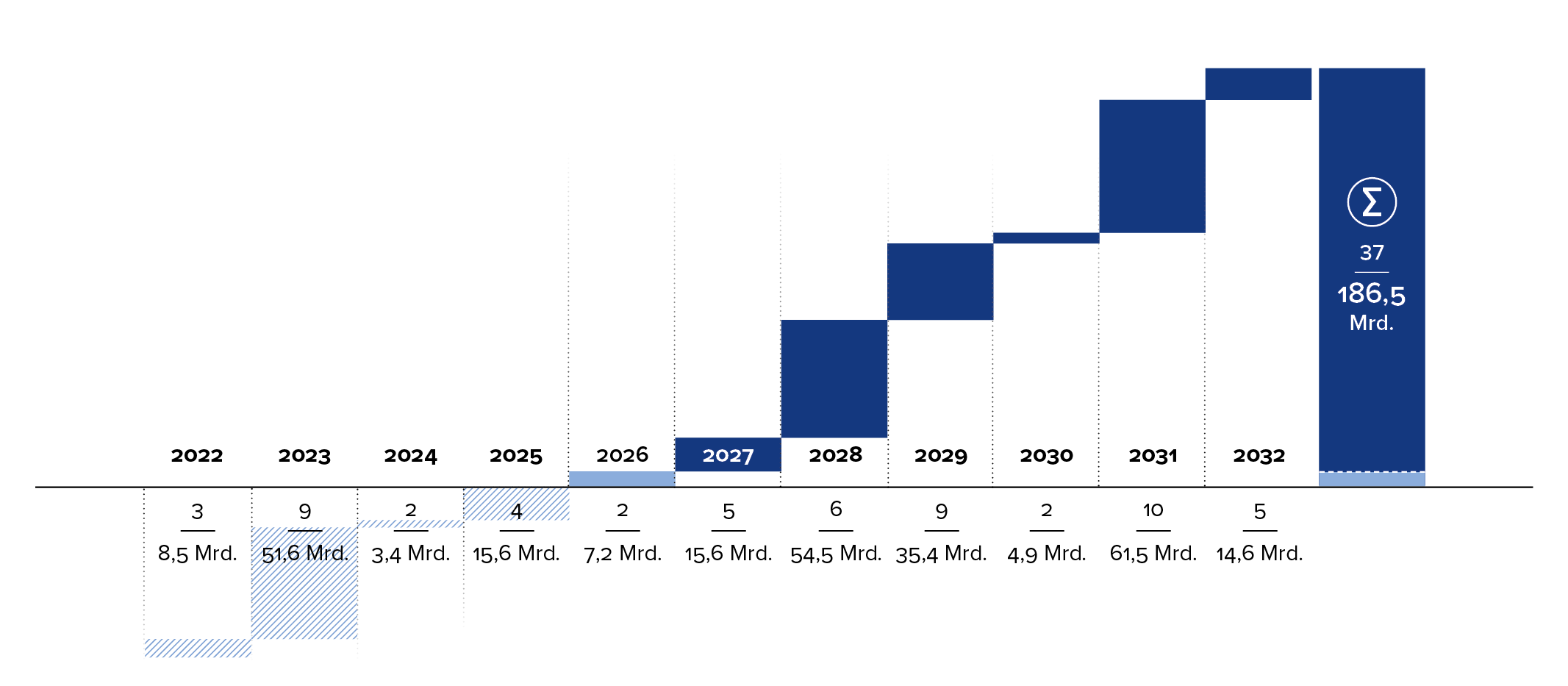
Diese Einsparungen schonen nicht nur die Gesundheitsbudgets, sondern sorgen in der Regel auch dafür, dass mehr Patientinnen und Patienten mit biologischen Wirkstoffen behandelt werden können. So tragen Biosimilars maßgeblich zur Demokratisierung medizinischer Innovationen bei. Diese Entwicklung wird sich noch verstärken, denn in den kommenden Jahren verlieren zahlreiche weitere umsatzstarke Biologika ihre Exklusivität. Bis 2032 sind darunter mehr als 30 Blockbuster-Medikamente, also Medikamente mit einem jährlichen globalen Umsatzvolumen jenseits von 1 Mrd. US$. Zusammengerechnet ergibt das ein Marktpotential von mehr als 180 Mrd. US$ – eine enorme Chance für Biosimilars.5
Der weltweite Umsatz mit den biologischen Nachfolgeprodukten soll Analysten zufolge im selben Zeitraum auf mehr als 74 Mrd. US$ ansteigen.
Formycon –
die Biosimilar Experten
Formycon hat es sich zur Aufgabe gemacht, eine treibende Kraft bei der Entwicklung von Biosimilars zu sein. Ziel des Unternehmens ist es, den Zugang für Patienten zu hocheffizienten Medikamenten zu demokratisieren und gleichzeitig zur finanziellen Entlastung der weltweiten Gesundheitssysteme beizutragen.
Mit seiner ausgewiesenen Expertise deckt Formycon die gesamte Wertschöpfungskette von der Entwicklung bis hin zur Lieferung des zugelassenen und vermarktungsfähigen Produktes ab. Die Kommerzialisierung der Biosimilars erfolgt weltweit in Zusammenarbeit mit etablierten Pharmaunternehmen, die sich auf die Vermarktung von Biosimilars in der jeweiligen geographischen Region spezialisiert haben.
Mit FYB201/Ranibizumab und FYB202/Ustekinumab sind bereits zwei Formycon-Biosimilars international verfügbar. FYB203/Aflibercept folgt im Laufe des Jahres 2026. Darüber hinaus besteht die Entwicklungspipeline aus vier weiteren Biosimilar-Kandidaten – darunter FYB206/Pembrolizumab und FYB208/Dupilumab.
Mehr über Biosimilars
Sie sehen gerade einen Platzhalterinhalt von YouTube. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von YouTube. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von YouTube. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr Informationen1 https://www.ema.europa.eu/en/human-regulatory-overview/biosimilar-medicines-overview
2 The path towards a tailored clinical biosimilar development, Schiestl et. al 2020
3 https://probiosimilars.de/publikationen/biosimilars-in-zahlen/
4 https://www.medicinesforeurope.com/wp-content/uploads/2025/03/Facts-and-figures-BIOS-2023-14-2-2025_Green.pdf
5 Quelle: EvaluatePharma-Datenbank, April 2022; Presseberichte; McKinsey-Analyse